徐國良研究組在《自然》雜志發(fā)文揭示維生素C參與產(chǎn)生一種全新的DNA修飾
來源:
時間:2019-05-05
5月2日���,國際學(xué)術(shù)權(quán)威期刊Nature在線發(fā)表了中國科學(xué)院生物化學(xué)與細(xì)胞生物學(xué)研究所徐國良研究組聯(lián)合多家單位合作完成的研究成果“A vitamin-C-derived DNA modification catalysed by an algal TET homologue”��。研究首次在萊茵衣藻(Chlamydomonas reinhardtii)這種單細(xì)胞真核生物中鑒定到一種新型的TET同源蛋白����,并發(fā)現(xiàn)該蛋白可以將維生素C的碳基骨架轉(zhuǎn)移到DNA上����,產(chǎn)生一種全新的DNA修飾���。文章詳細(xì)闡述了維生素C直接參與該DNA修飾的反應(yīng)機(jī)理,并揭示這一蛋白及其產(chǎn)生的DNA修飾在調(diào)節(jié)萊茵衣藻光合作用過程中的重要作用�。
徐國良研究組長期致力于DNA修飾酶和新修飾的發(fā)現(xiàn)工作,對哺乳動物DNA去甲基化過程中產(chǎn)生的DNA修飾及其生物學(xué)功能進(jìn)行了深入研究�。在真核生物中,DNA修飾的最主要形式是5-甲基胞嘧啶(5mC)���。近年來���,包括徐國良研究組在內(nèi)的三個實驗室發(fā)現(xiàn)TET雙加氧酶可以將5mC依次氧化產(chǎn)生5-羥甲基胞嘧啶 (5hmC)、5-醛基胞嘧啶 (5fC) ����、5-羧基胞嘧啶 (5caC)。后兩種修飾經(jīng)由胸腺嘧啶DNA糖苷酶(TDG)耦聯(lián)的堿基切除修復(fù)或DNA復(fù)制等途徑從基因組上被移除����,完成DNA去甲基化過程。但有關(guān)TET雙加氧酶在進(jìn)化過程中的保守性����,以及其在低等生物中的酶活與功能還有待進(jìn)一步探索。
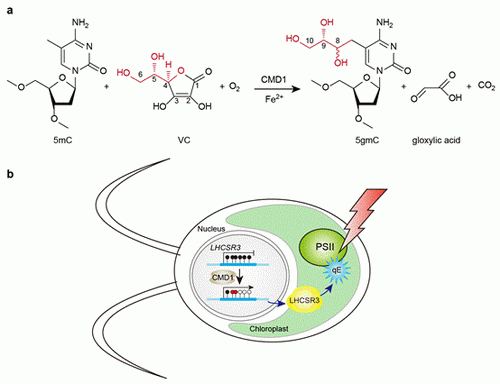
在最新發(fā)表的工作中�,研究者以萊茵衣藻作為模式生物,鑒定到了8個TET同源蛋白�。通過蛋白純化以及酶活分析,他們發(fā)現(xiàn)其中的CrTET1 可以將DNA上的5mC轉(zhuǎn)變?yōu)閮煞N不同的修飾堿基��,CrTET1也因此被重新命名為CMD1 (5-methylcytosine modification enzyme 1)����。進(jìn)一步的研究表明,這兩種新修飾都是在5mC的甲基碳上增加了一個甘油基����,二者由于空間結(jié)構(gòu)的差異而互為立體異構(gòu)體,因此將其統(tǒng)一命名為5-甘油基-甲基胞嘧啶(5gmC)���。這也是除了目前已知的5mC��、5hmC����、5fC�����、5caC、6mA�、5hmU和base J以外,在真核生物中發(fā)現(xiàn)的第8種DNA堿基修飾��。更加意外的是�,在研究5gmC上甘油基的來源時,研究者發(fā)現(xiàn)在傳統(tǒng)雙加氧酶反應(yīng)中所必需的α-酮戊二酸在CMD1酶催化反應(yīng)中可有可無�,取而代之的是另一個十分重要的小分子:維生素C。維生素C不僅通過提供電子參與CMD1的催化過程���,還直接將自身的甘油基團(tuán)轉(zhuǎn)移到5mC的甲基碳上����,形成新的DNA修飾����。研究者進(jìn)一步解析了CMD1催化5mC與維生素C反應(yīng)的化學(xué)機(jī)理,證實乙醛酸與二氧化碳為反應(yīng)的副產(chǎn)物����,從而揭示了一條全新的酶催化途徑。通過在萊茵衣藻中開發(fā)高效的基因編輯方法�����,研究者獲得了CMD1基因突變藻株。CMD1突變藻株在強(qiáng)光照射下的適應(yīng)能力明顯減弱����,這可能是由于CMD1突變造成一部分基因的甲基化水平升高���,使得包括與適應(yīng)強(qiáng)光有直接關(guān)系的LHCSR3在內(nèi)的多個基因的表達(dá)受到了抑制��,導(dǎo)致光合作用的負(fù)反饋調(diào)節(jié)作用減弱��。這項工作不僅首次報道了一種全新的DNA修飾5gmC��,同時報道了由維生素C介導(dǎo)的一種全新的酶活反應(yīng)類型���,闡述了CMD1及其催化產(chǎn)物5gmC在光合作用過程中的重要調(diào)控功能。這些研究豐富了研究人員對DNA修飾多樣性的認(rèn)識�。
生化與細(xì)胞所薛劍煌、陳國棟���、陳輝以及武漢物理與數(shù)學(xué)研究所豪富華為該論文的共同第一作者���。徐國良研究員、復(fù)旦大學(xué)生命科學(xué)學(xué)院唐惠儒教授以及中科院水生生物研究所黃開耀研究員為共同通訊作者。參與這項工作還有中科院生化與細(xì)胞所丁建平����、陳洛南,中科院有機(jī)所劉文�����、朱正江���,營養(yǎng)與健康研究所尹慧勇��,上海師范大學(xué)馬為民�����,德國RWTH Aachen University的Elmar Weinhold���,美國University of Pennsylvania的Rahul M. Kohli等數(shù)十個課題組。這項工作得到了中科院生化與細(xì)胞所分子平臺�、植生所質(zhì)譜平臺、馬普計算所計算生物學(xué)實驗技術(shù)平臺的大力支持�����,以及來自中科院、科技部和基金委的經(jīng)費(fèi)支持���。