陳勇研究組揭示MLL1甲基轉移酶復合物的組裝和活性調(diào)控新機制
來源:
時間:2019-09-27
9月23日����,國際學術期刊Nucleic Acids Research在線發(fā)表了中國科學院分子細胞科學卓越創(chuàng)新中心(生物化學與細胞生物學研究所)國家蛋白質(zhì)科學中心(上海)陳勇研究組的最新研究成果“The internal interaction in RBBP5 regulates assembly and activity of MLL1 methyltransferase complex”, 揭示了全長RBBP5參與MLL1甲基轉移酶復合物的組裝和活性調(diào)控的結構基礎和新的分子機制�。
組蛋白甲基化在許多生物學過程比如異染色質(zhì)的形成�����、X染色體的失活�����、轉錄調(diào)控中起到了重要的作用,其甲基化水平的異常能導致多種遺傳疾病和癌癥的發(fā)生發(fā)展���。在哺乳動物體內(nèi)����,組蛋白H3第4位賴氨酸的甲基化主要由MLL家族蛋白成員(MLL1/2/3/4, SET1A/B)共同行使。其中研究最多的是混合譜系白血病蛋白MLL1 (Mixed Lineage Leukemia 1)�,它能與70多種基因發(fā)生重排形成融合蛋白。產(chǎn)生的MLL1 融合蛋白因其復合物組裝和酶活異常�,造成機體的造血功能障礙而引發(fā)白血病。因此��,MLL1是一個潛在的白血病治療靶標�,研究其復合物的組裝和活性調(diào)控的分子機制有重大的意義和潛在的應用價值。
與其它甲基轉移酶家族不同�����,MLL家族甲基轉移酶的激活受到RBBP5�����、ASH2L���、WDR5這些輔助蛋白的共同調(diào)控���。其中���,RBBP5作為支架蛋白,在MLL1復合物的組裝和酶活調(diào)控中起到了巨大的作用��。陳勇研究組的前期工作揭示了RBBP5中的一段保守多肽(RBBP5AS+ABM)調(diào)控MLL家族蛋白活性的結構基礎和分子機制(Nature, 2016)���,但全長RBBP5蛋白參與MLL1甲基轉移酶復合物的組裝和活性調(diào)控的分子機制仍值得深入研究�����。
在陳勇研究員的指導下���,博士研究生韓建明、李婷婷等研究人員首次揭示了RBBP5存在內(nèi)部的相互作用����,并且這種相互作用會顯著增強MLL1復合物的活性。為找出該蛋白內(nèi)部發(fā)生相互作用的關鍵氨基酸��,研究人員解析了RBBP510-480高分辨的晶體結構�����。他們借助生化實驗鑒定出其內(nèi)部發(fā)生相互作用的關鍵氨基酸�����,并設計突變?nèi)テ茐膬?nèi)部相互作用后能顯著降低MLL1復合物的活性����。接著,研究人員運用生物小角散射技術���,揭示在溶液狀態(tài)中RBBP5內(nèi)部的相互作用可以使MLL1復合物的組裝更為緊湊�。反之����,若相互作用被破壞,則使其整體結構變得松散�����。令人驚喜的是����,研究人員經(jīng)序列分析首次揭示了RBBP5的C末端存在一個哺乳動物特有的CTD3 motif。經(jīng)生化實驗表明�����,富集賴氨酸的CTD3能高度親和核小體DNA,增強MLL1復合物與核小體的相互作用��,繼而促進復合物酶活的高效發(fā)揮����。若將這些賴氨酸全部突變?yōu)楸彼幔瑫魅鮉LL1復合物結合核小體的能力�,對其酶活發(fā)揮產(chǎn)生負調(diào)控。綜上�����,該研究成果揭示了全長RBBP5參與MLL1復合物組裝和活性調(diào)控的新機制����,為進一步研究MLL家族復合物的動態(tài)調(diào)控奠定了基礎。
生化與細胞所博士研究生韓建明為本文第一作者��,陳勇研究員為通訊作者����。感謝張江實驗室李娜博士、彭超博士����、華東理工大學全舒研究員的大力支持和幫助����。該研究得到張江實驗室國家蛋白質(zhì)科學研究(上海)設施BL19U1晶體衍射線站���、BL19U2小角散射線站、質(zhì)譜分析系統(tǒng)和規(guī)?�;鞍踪|(zhì)制備系統(tǒng)的大力支持和幫助���。該研究工作獲得中科院戰(zhàn)略性先導計劃和國家自然科學基金委的經(jīng)費資助��。
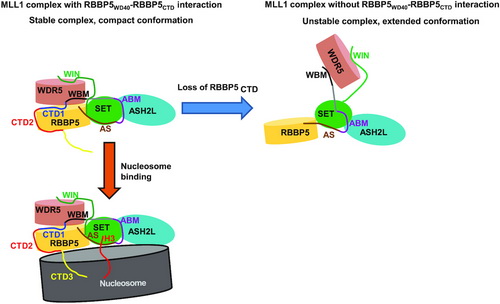
RBBP5調(diào)控MLL1復合物活性的結構模型
