李勁松研究組合作實(shí)現(xiàn)基于核移植技術(shù)的人類精子的體外擴(kuò)增
來(lái)源:
時(shí)間:2019-12-24
12月19日��,國(guó)際學(xué)術(shù)期刊Cell Research在線發(fā)表了中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心(生物化學(xué)與細(xì)胞生物學(xué)研究所)李勁松研究組和山東大學(xué)醫(yī)學(xué)院陳子江研究組��、北京大學(xué)未來(lái)基因診斷高精尖創(chuàng)新中心湯富酬研究組共同合作實(shí)現(xiàn)基于核移植技術(shù)體外擴(kuò)增人類精子的研究:“In vitro expansion of human sperm through nuclear transfer”。
該研究通過(guò)優(yōu)化的胚胎構(gòu)建策略和單倍體胚胎干細(xì)胞低氧建系策略首次建立了人類精子來(lái)源的孤雄單倍體胚胎干細(xì)胞系(AG-haESCs)�,證明了人類精子可以被重編程為孤雄單倍體胚胎干細(xì)胞,并發(fā)現(xiàn)人孤雄單倍體胚胎干細(xì)胞系(hAG-haESC)可以穩(wěn)定維持父源印記基因的特異性甲基化修飾模式���,可以在增殖和分化過(guò)程中保持單倍體倍性的穩(wěn)定���,因而可以作為父源遺傳物質(zhì)的替代物用于研究人類著床前胚胎發(fā)育的調(diào)控機(jī)制����。
二倍體核型是哺乳動(dòng)物細(xì)胞的主要核型���,單倍體細(xì)胞僅存在于雌雄生殖細(xì)胞發(fā)生的特定階段�����,而單倍體的生殖細(xì)胞由于處在終末分化狀態(tài)無(wú)法在體外實(shí)現(xiàn)增殖����。2011年劍橋大學(xué)(Leeb and Wutz,2011,Nature)和奧地利科學(xué)院(Elling et al.,2011,Cell Stem Cell)首次報(bào)道利用卵子孤雌激活結(jié)合流式分選技術(shù)(FACS)建立了哺乳動(dòng)物(小鼠)孤雌單倍體胚胎干細(xì)胞系���。2012年中科院生化所李勁松課題組(Yang et al.,2012,Cell)和動(dòng)物所周琪課題組(Li et al.,2012,Nature)首次報(bào)道建立了小鼠精子來(lái)源的AG-haESCs,并發(fā)現(xiàn)此類細(xì)胞可以支持產(chǎn)生半克隆小鼠�����,同時(shí)定義AG-haESCs為“人造精子細(xì)胞”�。“人造精子細(xì)胞”只具有一套遺傳物質(zhì)���,結(jié)合CRISPR/Cas9基因編輯工具可以在細(xì)胞水平和個(gè)體水平進(jìn)行復(fù)雜基因編輯和大規(guī)模的基因篩選�����。此后科學(xué)家繼續(xù)嘗試建立靈長(zhǎng)類動(dòng)物的單倍體胚胎干細(xì)胞�����,2013年李勁松研究組首次報(bào)道建立非人靈長(zhǎng)類動(dòng)物食蟹猴的孤雌單倍體胚胎干細(xì)胞系(Yang et al.,2013,Cell Res)���。2016年美國(guó)哥倫比亞大學(xué)團(tuán)隊(duì)(Sagi et al.,2016,Nature)和李勁松團(tuán)隊(duì)(Zhong et al.,2016,Cell Res)先后報(bào)道建立了人類卵子來(lái)源的孤雌單倍體胚胎干細(xì)胞系�。國(guó)內(nèi)外相關(guān)研究團(tuán)隊(duì)長(zhǎng)期致力于建立靈長(zhǎng)類動(dòng)物精子來(lái)源的孤雄單倍體胚胎干細(xì)胞�,但是均未取得成功,而靈長(zhǎng)類動(dòng)物包括人類的精子能否被重編程為孤雄單倍體胚胎干細(xì)胞也是長(zhǎng)期存在的疑問(wèn)����。
為了驗(yàn)證人類精子能否被重編程為人類胚胎干細(xì)胞, 研究團(tuán)隊(duì)采用了細(xì)胞骨架非破壞性的核移植策略構(gòu)建了人孤雄胚胎����,即受精后通過(guò)預(yù)激活然后去除第二極體(PB2)和前原核(PPN)的方式去除母源遺傳物質(zhì)(圖1)。經(jīng)過(guò)傳統(tǒng)的胚胎干細(xì)胞系(正常氧環(huán)境21% O2)建系����,發(fā)現(xiàn)得到的細(xì)胞系全部為二倍體(5/5)。而此前有研究報(bào)道低氧培養(yǎng)環(huán)境有利于人胚胎干細(xì)胞的干性維持和小鼠EpiLC(小鼠表胚層樣細(xì)胞)的建立�,并且研究團(tuán)隊(duì)發(fā)現(xiàn)5% O2有助于單倍體干細(xì)胞單倍體的維持����?;诖耍瑘F(tuán)隊(duì)推測(cè)低氧環(huán)境可能有利于人孤雄單倍體胚胎干細(xì)胞系的建立�,并利用新的建系環(huán)境成功建立了兩株hAG-haESCs,發(fā)現(xiàn)在培養(yǎng)過(guò)程和體內(nèi)體外分化過(guò)程中hAG-haESCs的單倍體倍性均保持相對(duì)穩(wěn)定���。
同時(shí)�����,研究團(tuán)隊(duì)通過(guò)全基因組DNA甲基化測(cè)序(WGBS)和轉(zhuǎn)錄組測(cè)序(RNA-seq)揭示了hAG-haESCs具有與精子類似的印記基因修飾模式和表達(dá)模式�,尤其是在對(duì)于胚胎發(fā)育至關(guān)重要的H19-DMR和IG-DMR上保持了嚴(yán)格的父源印記修飾特征(圖2)�����,而這一特征在此前建立的小鼠“人造精子細(xì)胞”中是不存在的���,這暗示了hAG-haESCs支持胚胎發(fā)育的能力。進(jìn)一步����,研究人員利用hAG-haESCs代替精子對(duì)卵子進(jìn)行“授精”����,結(jié)果發(fā)現(xiàn)重構(gòu)的胚胎可以成功發(fā)育到囊胚并可建立胚胎干細(xì)胞系��。結(jié)合單細(xì)胞轉(zhuǎn)錄組測(cè)序技術(shù)(single-cell RNA-seq)揭示了hAG-haESCs來(lái)源的胚胎和精子受精來(lái)源的胚胎高度相似(圖3)��。這項(xiàng)研究論證了人類精子可以重編程為單倍體胚胎干細(xì)胞���,為將來(lái)的生命科學(xué)和生殖醫(yī)學(xué)研究提供了前瞻性的技術(shù)儲(chǔ)備��。
分子細(xì)胞中心博士生張曉宇��、北京大學(xué)未來(lái)基因診斷高精尖創(chuàng)新中心博士生鄭宇軒����、山東大學(xué)醫(yī)學(xué)院教授吳克良和教授趙涵為共同第一作者�,分子細(xì)胞中心李勁松研究員、山東大學(xué)陳子江院士��、北京大學(xué)未來(lái)基因診斷高精尖創(chuàng)新中心湯富酬教授為共同通訊作者�。該研究得到分子細(xì)胞中心細(xì)胞分析技術(shù)平臺(tái)和基因組標(biāo)簽計(jì)劃研發(fā)中心的大力支持,同時(shí)該研究還得到國(guó)家自然科學(xué)基金委�����、國(guó)家科技部和中國(guó)科學(xué)院以及上海市的經(jīng)費(fèi)資助。
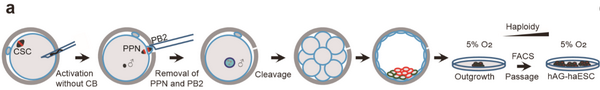
圖1:人孤雄單倍體胚胎干細(xì)胞系(hAG-haESC)的建系流程
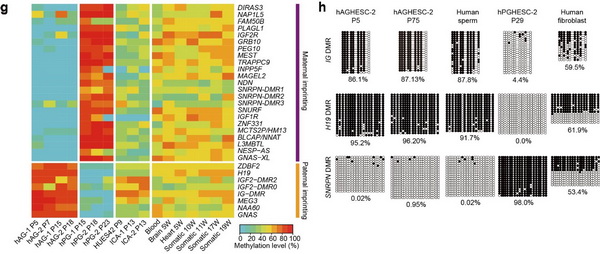
圖2:hAG-haESCs穩(wěn)定維持父源印記基因DNA甲基化模式
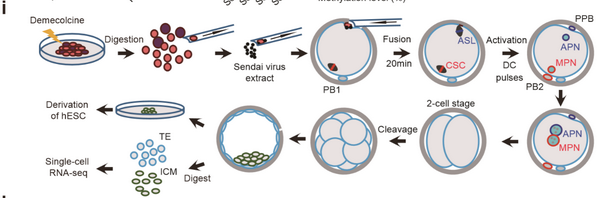
圖3:利用hAG-haESCs代替精子來(lái)對(duì)卵子進(jìn)行“授精”


