李勁松、胡蘋合作利用“人造精子細(xì)胞”介導(dǎo)半克隆技術(shù)構(gòu)建出新型Ⅰ型強直性肌營養(yǎng)不良癥小鼠模型
來源:
時間:2020-02-11
2月5日�����,中國科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心(生物化學(xué)與細(xì)胞生物學(xué)研究所)李勁松研究組、胡蘋研究組合作的文章“Dosage effect of multiple genes accounts for multisystem disorder of myotonic dystrophy type 1”在國際學(xué)術(shù)期刊《細(xì)胞研究》上作為封面文章發(fā)表�。該研究利用“人造精子細(xì)胞”介導(dǎo)的半克隆技術(shù),快速構(gòu)建多基因雜合突變小鼠模擬人Ⅰ型強直性肌營養(yǎng)不良癥(DM1)的多基因劑量不足效應(yīng)����,成功地在小鼠中再現(xiàn)了DM1的大部分病癥,為開展DM1致病機制和藥物篩選研究提供了新模型���。
人I型強直性肌營養(yǎng)不良癥(DM1)是一種遺傳性疾病,是由肌營養(yǎng)不良癥肌強直蛋白激酶(DMPK)基因3’UTR區(qū)CTG重復(fù)序列的異常擴增引起的復(fù)雜疾病����。正常人的CTG短串聯(lián)重復(fù)序列平均為37個��,DM1患者的CTG超過50個����。DM1嚴(yán)重程度和發(fā)病年齡與CTG的數(shù)量有關(guān)�,主要癥狀包括肌強直、肌萎縮��、肌無力����、心臟缺陷、白內(nèi)障等����。隨著重復(fù)序列的異常增加(~4000),可產(chǎn)生新生兒呼吸衰竭��,心臟發(fā)育不全等���,甚至造成新生兒致死(先天性DM1, CDM)���。重復(fù)序列的異常增加不僅影響DMPK的mRNA和蛋白水平(基因單倍劑量不足效應(yīng))�,同時也改變了鄰近染色質(zhì)的結(jié)構(gòu)并降低SIX5和DMWD的表達(dá)(局部染色質(zhì)結(jié)構(gòu)改變效應(yīng))��。此外����,許多研究還表明異常延遲的DMPK mRNA會滯留在核內(nèi),并募集了剪接調(diào)控因子�,如MBNL1,在核內(nèi)形成核糖核聚集體(病灶)����,引起RNA毒性(RNA毒性效應(yīng))。然而��,單基因純合突變小鼠模型(包括Dmpk�、Six5和Mbnl1)均不能模擬DM1患者的大部分癥狀,更不能模擬出CDM1的癥狀�����,提示重復(fù)序列的異常擴增導(dǎo)致多基因的表達(dá)的同時下降可能是DM1復(fù)雜病癥產(chǎn)生的原因���,但是到目前為止仍然缺乏直接的實驗證據(jù)�。
為了驗證這一假說����,研究團(tuán)隊利用李勁松課題組建立的孤雄單倍體胚胎干細(xì)胞(AG-haESCs)能夠替代精子產(chǎn)生小鼠的半克隆技術(shù)(又稱為“人造精子細(xì)胞”介導(dǎo)半克隆技術(shù)),結(jié)合CRISPR/Cas9基因編輯技術(shù)�,成功構(gòu)建了三基因(Dmpk, Six5, Mbnl1)敲除的“人造精子細(xì)胞”系,并通過卵子注射一步獲得攜帶三基因雜合敲除的半克隆小鼠(Dmpk+/-; Six5+/-; Mbnl1+/-)�����。表型分析發(fā)現(xiàn)該小鼠產(chǎn)生了典型的DM1表型���,包括四月齡時出現(xiàn)的肌肉無力�、肌肉萎縮�、嚴(yán)重的運動障礙;小腸和膈肌結(jié)構(gòu)異常(消化和呼吸功能障礙)���; 12個月齡小鼠出現(xiàn)心肌纖維結(jié)構(gòu)異常(心臟功能障礙)等���。
三基因雜合敲除的小鼠可以作為一種新的DM1模型,模擬DM1成年患者中觀察到的大多數(shù)病理表型���,說明DM1中出現(xiàn)的病理表型的確是由多個基因劑量下降協(xié)同產(chǎn)生的����。然而,該小鼠沒有出現(xiàn)CDM的表型���,提示其它基因的劑量變化可能與此有關(guān)����。為此����,研究人員進(jìn)一步構(gòu)建了Dmwd+/-半克隆小鼠(Dmpk的上游基因,有報道顯示患者中DMWD的表達(dá)水平下降)�����,表型分析發(fā)現(xiàn)該小鼠出現(xiàn)肌肉萎縮的表型����,說明Dmwd的確與DM1的表型有關(guān)。
團(tuán)隊進(jìn)一步將帶有四基因(Dmpk, Six5, Mbnl1, Dmwd)敲除的“人造精子細(xì)胞”注射到卵子中產(chǎn)生了四基因雜合敲除的小鼠(Dmpk+/-; Six5+/-; Mbnl1+/-; Dmwd+/-)���。與三基因雜合敲除的小鼠相比�����,四基因雜合敲除的半克隆小鼠呈現(xiàn)出先天性DM1表型:出生后幾個小時內(nèi)就出現(xiàn)大約22%的死亡���,肺擴張失敗是導(dǎo)致四基因雜合敲除半克隆幼仔出生后死亡的主要原因���,而導(dǎo)致肺擴張失敗的原因可能是膈肌發(fā)育異常�����;存活下來的小鼠出現(xiàn)嚴(yán)重的肌強直�����、肌無力��、肌肉萎縮和運動缺陷��;部分小鼠出現(xiàn)嚴(yán)重的腸道異常和心臟發(fā)育異常�����,約46%小鼠在斷奶前死亡�;剩下的小鼠可以發(fā)育至成年,呈現(xiàn)出典型的DM1表型�����,包括白內(nèi)障等。
進(jìn)一步研究發(fā)現(xiàn)三基因和四基因雜合敲除小鼠的肌肉干細(xì)胞數(shù)量以及增殖能力與對照無差異�����,然而其干性降低��,從而導(dǎo)致了肌肉分化的缺陷��。利用這一特點�����,研究人員建立了促進(jìn)肌肉干細(xì)胞分化的小分子篩選系統(tǒng)�����,并發(fā)現(xiàn)了一種在細(xì)胞水平上能緩解肌肉分化異常表型的小分子化合物�����,為進(jìn)一步開展大規(guī)模DM1藥物篩選研究奠定了基礎(chǔ)�����。
該研究通過利用“人造精子細(xì)胞”介導(dǎo)半克隆技術(shù)快速構(gòu)建多基因劑量下調(diào)小鼠模型模擬出DM1的多數(shù)病癥,提供了直接證據(jù)支持CTG重復(fù)序列的異常擴增導(dǎo)致多個基因表達(dá)水平變化(下調(diào))從而誘發(fā)DM1的復(fù)雜病理表型的假說���;同時���,這些模型的建立為深入研究DM1的發(fā)病機理和進(jìn)行藥物篩選奠定了基礎(chǔ)。
美國貝勒醫(yī)學(xué)院人類遺傳學(xué)家Richard H. Finnell教授在同期刊發(fā)了評論文章����,認(rèn)為該研究為人強直性肌營養(yǎng)不良癥研究和治療提供了可靠的小鼠模型���,解決了該領(lǐng)域長期缺乏有效小鼠模型的困境���;肯定了半克隆技術(shù)結(jié)合CRISPR/Cas9基因編輯技術(shù)產(chǎn)生多基因雜合突變小鼠模型的高效性及有效性;并認(rèn)為此技術(shù)有望成為包括出生缺陷����、衰老、心血管����、癌癥、神經(jīng)發(fā)育相關(guān)疾病在內(nèi)復(fù)雜型疾病的一個強有力研究工具�。
尹奇、王紅葉、李鈉����、丁一夫、謝振飛和金立方為本文的共同第一作者�,李勁松研究員和胡蘋研究員為共同通訊作者。本工作得到了中國科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心(生物化學(xué)與細(xì)胞生物學(xué)研究所)鮑嵐研究員����、周斌研究員、福建醫(yī)科大學(xué)陳萬金教授的大力支持���,該研究受到了分子細(xì)胞中心化學(xué)生物學(xué)技術(shù)平臺��、細(xì)胞分析技術(shù)平臺����、實驗動物技術(shù)平臺和基因組標(biāo)簽計劃研發(fā)中心的大力支持�����,同時還得到國家自然科學(xué)基金委�����、國家科技部、上海市科委和中國科學(xué)院的經(jīng)費資助���。
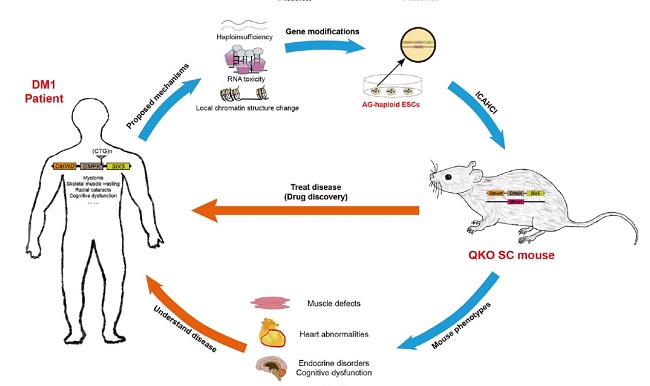
DM1小鼠模型的構(gòu)建及其潛在應(yīng)用


