Nature發(fā)表?xiàng)钗【S研究組合作成果:揭示尿苷二磷酸葡萄糖抑制肺癌轉(zhuǎn)移的新功能
來源:
時(shí)間:2020-03-23
北京時(shí)間6月27日凌晨,國際權(quán)威學(xué)術(shù)期刊Nature在線發(fā)表了中國科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心/生物化學(xué)與細(xì)胞生物學(xué)研究所楊巍維研究組的最新研究成果:“UDP-glucose accelerates SNAI1 mRNA decay and impairs lung cancer metastasis”�����。研究首次揭示了糖醛酸代謝通路中的尿苷二磷酸葡萄糖(UDP-Glc)抑制肺癌轉(zhuǎn)移的新功能及作用機(jī)制���,為肺癌轉(zhuǎn)移的監(jiān)測和阻斷提供了新的靶點(diǎn)和生物標(biāo)志物。
肺癌是全世界也是我國發(fā)病率和死亡率最高的惡性腫瘤�����。我國每年肺癌發(fā)病人數(shù)超過73萬�,死亡人數(shù)超過61萬,五年生存率低至16.1%����,肺癌已然成為“第一大癌癥”與“頭號癌癥殺手”。轉(zhuǎn)移是肺癌死亡率居高不下的重要原因�����。傳統(tǒng)手術(shù)以及術(shù)后放化療可以很好的控制原發(fā)腫瘤��,但對發(fā)生轉(zhuǎn)移的腫瘤往往束手無策���。初步統(tǒng)計(jì)�,95%以上的腫瘤死亡是由腫瘤轉(zhuǎn)移造成的�。因此,深入理解腫瘤轉(zhuǎn)移的分子機(jī)制不僅有助于腫瘤早期轉(zhuǎn)移的發(fā)現(xiàn)�,還將為腫瘤轉(zhuǎn)移的阻斷提供新的策略,并最終改善癌癥患者的預(yù)后�����。
代謝異常是惡性腫瘤的重要特征�。癌癥相關(guān)基因的突變造成了細(xì)胞內(nèi)多條信號通路的改變,從而影響腫瘤細(xì)胞的代謝���,并重塑腫瘤細(xì)胞�����,以增強(qiáng)其存活和生長能力�。實(shí)際上,腫瘤細(xì)胞需要改變代謝的狀態(tài)來應(yīng)答癌基因信號通路傳遞的增殖信號����。除此之外,異常的腫瘤微環(huán)境也能進(jìn)一步改變腫瘤細(xì)胞的代謝表型�,從而影響腫瘤的發(fā)生發(fā)展及對治療的反應(yīng)性。然而���,這些異常的代謝如何支撐腫瘤轉(zhuǎn)移卻鮮為人知�����。
楊巍維研究組長期圍繞腫瘤代謝異常功能與調(diào)控機(jī)制�,重點(diǎn)關(guān)注腫瘤代謝與信號轉(zhuǎn)導(dǎo)的交互調(diào)控���,旨在揭示腫瘤細(xì)胞代謝重編程在腫瘤發(fā)生發(fā)展中的功能及調(diào)控機(jī)制���,為癌癥的診治、藥物研發(fā)等提供理論依據(jù)及研究基礎(chǔ) (Nature 2011, Cell 2012, Mol Cell 2012, Nat Cell Biol, 2013, Cell Res 2017, Mol Cell 2018, PLOS Biol 2018, Nat Commun 2016, 2019)�����。
在該項(xiàng)研究中,他們發(fā)現(xiàn)在表皮生長因子受體(EGFR)激活的條件下�����,尿苷二磷酸葡萄糖脫氫酶(UGDH)第473位酪氨酸(Y473)發(fā)生了磷酸化��。UGDH是糖醛酸途徑的限速酶��,可以催化UDP-Glc反應(yīng)生成尿苷二磷酸葡萄糖醛酸(UDP-GlcUA)��;后者可以作為細(xì)胞合成糖胺聚糖的原料(圖1)�����。磷酸化的UGDH可與HuR結(jié)合�����,并將UDP-Glc轉(zhuǎn)化為UDP-GlcUA��,從而削弱了UDP-Glc對HuR與SNAI1 mRNA結(jié)合的抑制��,增強(qiáng)了SNAI1 mRNA穩(wěn)定性及蛋白表達(dá)�����;SNAI1表達(dá)的升高增強(qiáng)了腫瘤細(xì)胞遷移能力�����,進(jìn)而促進(jìn)了肺癌轉(zhuǎn)移(圖2)�。
此外,UDP-Glc水平與肺癌患者的轉(zhuǎn)移復(fù)發(fā)密切相關(guān)��。研究者發(fā)現(xiàn)���,相比原發(fā)灶�,轉(zhuǎn)移灶中肺癌組織的UDP-Glc水平急劇降低�;更為重要的是,發(fā)生遠(yuǎn)端轉(zhuǎn)移的肺癌患者的血液樣本中含有更低的UDP-Glc水平�����。此外�,他們還發(fā)現(xiàn)肺癌組織中UGDH Y473磷酸化水平越高,發(fā)生肺癌轉(zhuǎn)移的幾率越大����,且患者的預(yù)后越差。
本研究揭示了UDP-Glc抑制腫瘤的新功能�����,建立了代謝小分子調(diào)控蛋白質(zhì)功能的新模式,建立了細(xì)胞代謝與RNA穩(wěn)定性調(diào)控的新連接�,為肺癌轉(zhuǎn)移的診斷和治療提供了首個(gè)生化標(biāo)志物及干預(yù)新策略。
本研究主要由中國科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心/生物化學(xué)與細(xì)胞生物學(xué)研究所楊巍維研究組與大連化學(xué)物理研究所李國輝研究組合作完成��。廣州大學(xué)副教授王雄軍����、生化與細(xì)胞所博士生劉瑞隆��、朱文成����、大連化物所楚慧郢為本文共同第一作者,楊巍維研究員和李國輝研究員為該論文的共同通訊作者�。該項(xiàng)工作得到了生化與細(xì)胞所程紅研究員、高棟實(shí)驗(yàn)室博士生李飛的指導(dǎo)與支持�����。該研究得到國家自然科學(xué)基金委���、中國科學(xué)院的資助�,數(shù)據(jù)收集工作得到生化與細(xì)胞所公共技術(shù)服務(wù)中心分子平臺、細(xì)胞平臺����、化學(xué)平臺、動(dòng)物平臺和GTP中心的支持���。
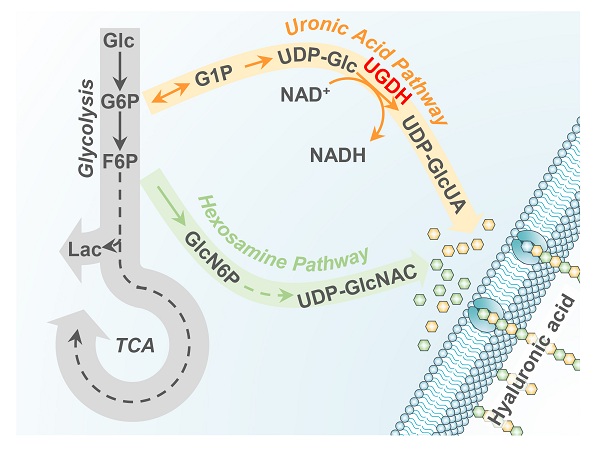
圖1 糖醛酸途徑
糖醛酸途徑是糖酵解的分支通路�。糖醛酸途徑的原料來自于糖酵解的中間代謝產(chǎn)物葡萄糖6-磷酸���。經(jīng)過幾步反應(yīng)最終生成UDP-葡萄糖醛酸�。UDP-葡萄糖醛酸與己糖胺途徑(Hexosamine Pathway)生成的UDP-乙酰氨基葡萄糖一起用于糖胺聚糖����,如透明質(zhì)酸(Hyaluronic Acid, HA)等物質(zhì)的生物合成。
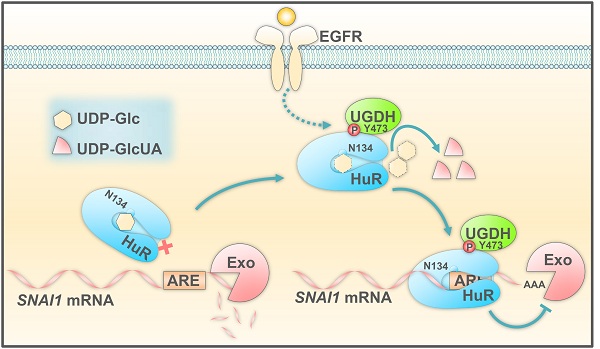
圖2 UDP-Glc調(diào)控肺癌轉(zhuǎn)移的模型
UDP-Glc與RNA結(jié)合蛋白HuR相互作用�,競爭性抑制HuR對SNAI1 mRNA的穩(wěn)定效應(yīng),從而抑制肺癌轉(zhuǎn)移���;EGFR信號激活可促使UGDH與HuR結(jié)合�����,并將UDP-Glc轉(zhuǎn)化為UDP-GlcUA�,從而解除了它對肺癌轉(zhuǎn)移的抑制。